1,294 읽음
노화된 망막세포에만 표적 약물…"황반변성 새 치료법"
 와이드경제
와이드경제 1
1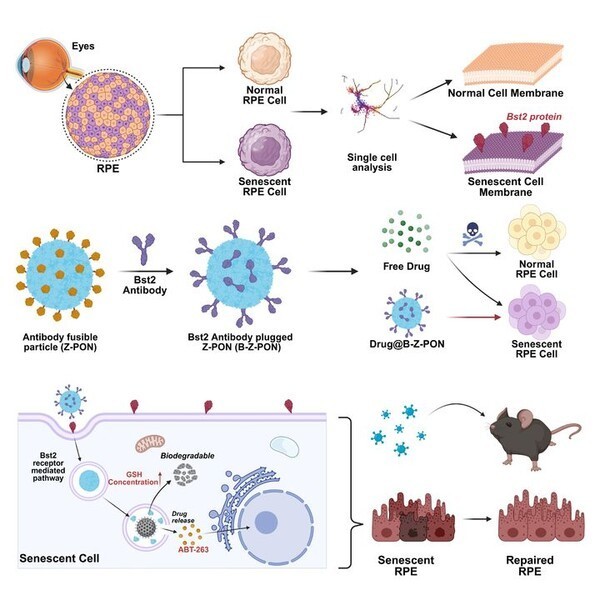
울산과학기술원(UNIST)은 화학과 유자형 교수와 건국대병원 안과 정혜원 교수팀이 노화된 망막색소상피세포(RPE)만 골라서 제거 약물을 전달하는 나노 입자를 개발해, 실험쥐의 시각 기능을 일부 회복하는 성과를 거뒀다고 9일 밝혔다.
망막색소상피세포의 노화는 건성 노인성 황반변성의 주요 원인으로 지목되고 있다. 노화 상태에 접어든 RPE는 단순히 기능을 멈춘 세포가 아니라, 주변에 독성 염증 물질을 뿜어내며 건강한 정상 세포까지 파괴하는 역할을 하기 때문이다. 최근 이 노화 세포를 제거할 수 있는 세놀리틱스(Senolytics) 계열 약물이 주목받고 있지만, 정상 세포에 이 약물이 들어가면 독성 부작용이 일어난다.
연구진이 개발한 나노입자는 노화 세포에만 이 약물을 전달하는 역할을 한다. 노화 RPE는 표면에 Bst2라는 단백질이 많은데, 나노입자 겉면에 이 단백질에만 결합하는 특이 항체를 장착했기 때문이다. 노화 RPE 세포에 도달한 나노입자는 세포 안쪽으로 들어가 분해되면서, 내부에 들어있던 노화 세포 사멸 약물(ABT-263)을 방출한다. 혹시 나노입자가 정상 세포에 오배달되더라도, 노화 세포 특유의 고농도 글루타치온 환경에서만 분해가 일어나게 설계돼 안전하다.
노화된 RPE 표면에 Bst2라는 단백질이 많다는 점도 이번 연구를 통해 처음으로 밝혀졌다. 연구진은 자연 노화 쥐와 화학 약물로 병리적 노화를 유도한 쥐의 유전자 데이터를 교차 분석해, 노화 세포 표지자로서 Bst2를 발굴해 냈다.
개발된 나노입자에 약물을 담아 쥐의 안구에 주사한 결과, 정상 세포 손상 없이 노화 세포만 제거됐으며, 빛에 대한 전기적 반응(망막 전위도)이 유의미하게 커지며 시각 기능이 회복되는 것을 확인했다.
정혜원 교수는 "증상 완화에 머물렀던 기존 치료 방식과 달리, 질환의 출발점 자체를 겨냥했다는 점에 차별점이 있다"며 "마땅한 표준치료법이 없는 건성 노인성 황반변성에서 새로운 치료 접근이 될 수 있을 것으로 기대한다"고 말했다.
유자형 교수는 "노화세포 표면에만 나타나는 단백질을 새롭게 발굴해 노화세포만을 표적하는 약물 전달 나노입자를 설계할 수 있었다"며 "나노입자 표면의 특이 항체만 교체하면 다른 노인성 질환 노화세포 표적 치료에 활용 가능할 것"이라고 밝혔다.
이번 연구는 과학기술정보통신부 한국연구재단(NRF)과 보건복지부 한국보건산업진흥원(KHIDI)의 한국형 ARPA-H 프로젝트 등의 지원을 받아 수행됐으며, 결과는 국제학술지 네이처 커뮤니케이션즈(Nature Communications)에 3월 18일자로 게재됐다.
